你真的理解保形性了吗?深度揭秘 ALD 薄膜生长中的常见概念 !
时间:2024-10-08 阅读:708
研究原子层沉积 (ALD) 生长的薄膜的保形性不仅从应用角度来看很有趣。它还可以提供有价值的基本信息,如有关反应概率的信息。研究薄膜保形性也被证明是提升等离子体 ALD 一种有效的方法。本篇文章内容来自K. Arts, W.M.M. Kessels 和 H.C.M Knoops 的研究,为大家深度揭秘与优化 ALD 薄膜生长的保形性。
通过表面吸附和表面复合而损失的反应物分子看起来可能相似,但会导致非常不同的生长行为。本篇文章将从三个方面解释这一现象,并希望通过具象的案例图片和动画演示来帮助大家理解反应、扩散和复合限制生长等概念以及在(等离子) ALD 过程中优化薄膜保形性。
01.模拟 ALD 保形性:扩散、吸附和复合
要将 ALD 过程中的薄膜保形性与反应概率等基本参数联系起来,我们需要一个数值或分析模型来描述生长过程。Cremers 等人最近在研究中已经报道了几种这样的模型,其中许多模型受到 Gordon 在 2003 年提出的分析模型的启发。
该模型可以充分预测在扩散限制生长的情况下保形涂覆高纵横比 (高 AR) 孔所需的最小反应物剂量(下一节将解释),无需深入研究已报告模型的细节。值得一提的是,这些模型本质上都是模拟一个 ALD 半周期内获得的表面覆盖率θ。从实验上讲,这种表面覆盖率或“可用吸附位点的反应分数”可以与每周期生长率 (GPC) 相关联,因此与沉积膜的厚度有关,如图 1 所示。
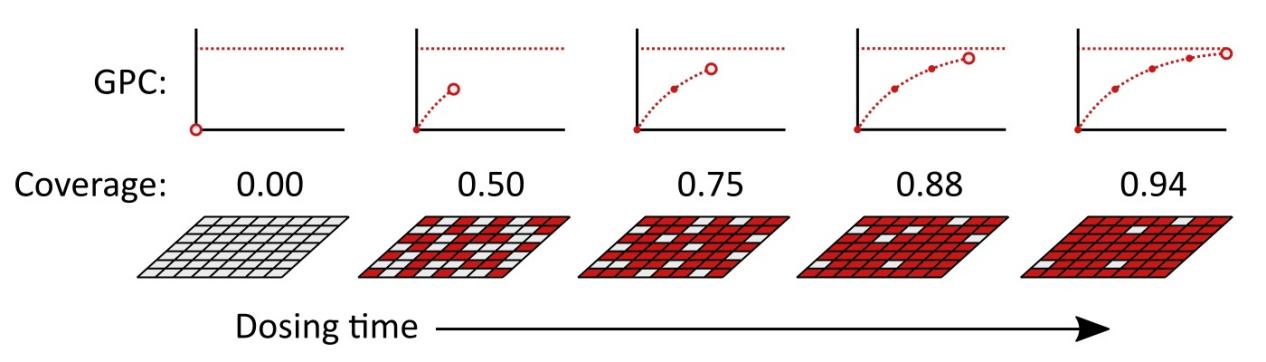
图1:表面覆盖率θ:在一个 ALD 半周期内,表面覆盖率和 GPC 与给药时间的关系。
在本篇文章中,我们将重点介绍使用 Arts, K 在研究中使用的模型所获得的结果,该连续模型由两个耦合方程组成:(1) 描述不可逆吸附的著名朗缪尔方程;(2) 用于计算高 AR 结构内气相反应物密度的一维扩散方程。
气相反应物分子的不可逆吸附用粘附概率 S 来描述:反应物分子在碰撞时不可逆吸附或“粘附”到表面的概率。注意,当表面覆盖率 等于 1 时,这个概率在饱和状态下应该为零。如果不是,生长将继续,我们模拟的是化学气相沉积 (CVD) ,而不是 ALD。
在采用的 Langmuir 模型中,使用 S=S0(1-θ) 来模拟 ALD 的自终止行为。这里,S0 是初始粘附概率:在模拟半周期的反应物之前对应起始表面的粘附概率。根据 ALD 工艺的不同,初始粘附概率通常在 10-5 到 10-1 范围内。这意味着在发生不可逆吸附之前,反应物分子可以与表面碰撞约 10 到 100,000 次。
除了吸附,气相反应物物种也可以通过复合从表面脱附,如通过等离子体 ALD ,反应性自由基可以复合形成稳定的分子,但这些分子不会作用于薄膜生长。例如,原子氧(O)可以复合形成稳定的分子 O2。同样,在基于臭氧的 ALD 过程中,反应性臭氧也可以通过表面反应形成分子 O2 而丢失。在这两种情况下,这种损失通道是使用表面复合概率r来模拟的:反应物分子(或原子)在与表面碰撞时复合的概率。与前驱体或共反应物的初始粘附概率类似,等离子体自由基的表面复合概率通常在10-5到10-1的范围内。
“吸附损失”和“复合损失”之间有两个主要区别,如图 2(IIa和 IIb)所示。首先,吸附反应会导致薄膜生长,从而增加表面覆盖率,而复合反应则不会。其次,当接近饱和时,吸附损失会停止,这样反应物分子就可以扩散到高纵横比更深的地方,直到找到可用的未反应吸附位点。相比之下,复合损失在结构中的任何地方都会继续发生,因此往往占主导地位。
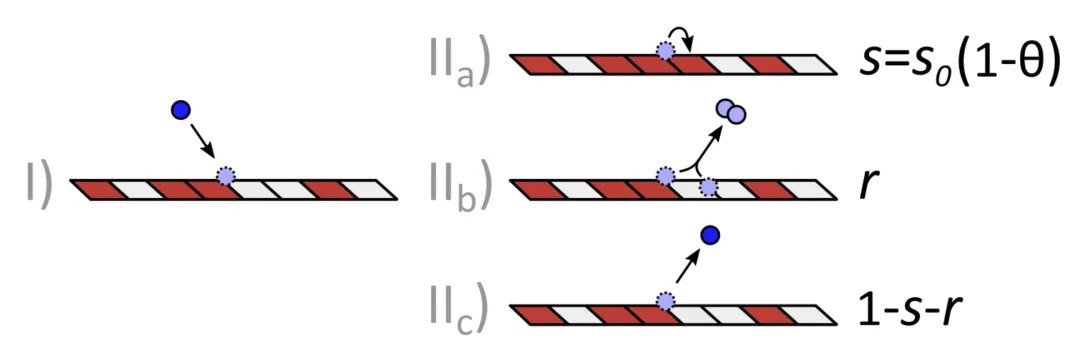
图 2:(等离子) ALD 过程中气相反应物(蓝色圆圈)与表面之间的模拟相互作用图,其中方块代表空的(白色)和已占用的(红色)吸附位点。当反应物分子或原子撞击表面 (I) 时,它可以吸附在空的吸附位点 (IIa ),与表面上的另一个原子重新结合 (IIb ) 或反射 (IIc )。只有吸附 (IIa ) 才能增加表面覆盖率。
初始粘附概率 S0 和复合概率r是决定生长机制和最终薄膜保形性的重要参数。下面将讨论这些不同的生长机制,其中模拟结果假设为“单粒子”,自由分子在狭窄的沟槽中扩散(即间隙高度h≤沟槽宽度,见图3)。虽然实际情况通常更为复杂,考虑到气相碰撞、复杂的 3D 几何形状等,但总体行为本质上是通用的,通常在低压力下(例如,对于微米级孔或沟槽的压力<1托)是现实的。
02.热ALD:反应限制生长与扩散限制生长
对于热驱动 ALD 而言,复合通常不起作用 ( r=0),我们可以区分两种不同的生长机制:反应限制生长和扩散限制生长。图3说明了反应限制生长和扩散限制生长之间的差异。在反应限制生长(左)中,气相反应分子的吸附所需的时间比这些分子扩散到高 AR 结构中所需的时间更长。在扩散限制生长(右)中,反应物分子在它们扩散到结构末端之前就已经吸附了。根据此描述您可能会猜到,扩散时间 tdiff 与吸附时间 tads之间的比率决定了薄膜生长是反应限制的( tdiff/tad≤1) 还是扩散限制的 (tdiff/tads≥1)。
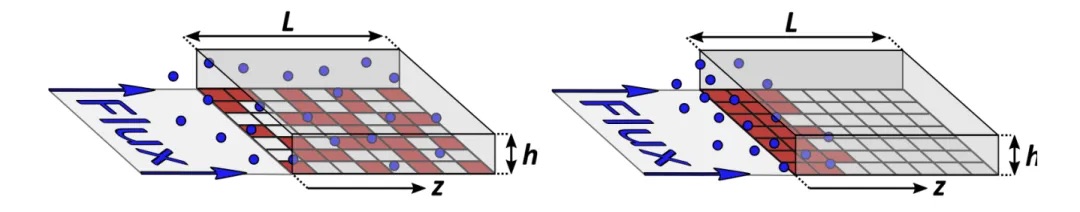
图 3:反应限制生长(左)和扩散限制生长(右)的图示
这里,我们使用扩散时间作为反应物分子扩散到高 AR 结构末端所需的时间。对于时间t内的“随机游走”扩散,反应物分子的平均穿透深度随着 √t而增加。相应地,到达结构末端所需的时间随着纵横比的平方而增加,所以tdiff ∝ AR2,其中AR = L/h。
吸附时间是指“填满”一定比例的吸附位点所需的时间。无论这个比例是多少(1/e、0.5、0.9999……),吸附时间都与发生吸附反应所需的平均碰撞次数成正比。在最初的空表面上,这个碰撞次数等于 1/S0,因此,它成立 tads ∝ 1/S0。
对于沟槽中的分子扩散,扩散时间与吸附时间之比可以通过 tdiff/tads =3/4 S0(L/h)2 或更粗略地计算为 tdiff/tads≈S0AR2。虽然正式推导并不那么简单,但可以使用比例 tads ∝ AR2 和 tads ∝ 1/S0 上述解释来理解这个表达式。对于 S0AR2的低值,大致当S0AR2 < 1时,扩散比吸附快得多,并且我们有反应限制的增长。另一方面,当S0AR2 > 100 时,薄膜生长受到扩散限制。
我们现在将使用下面的动画来讨论这两种情况,动画展示了沟槽中 ALD 的横截面侧视图。这里,为了清晰起见,并为了与我们实验中使用的PillarHall™ 横向高纵横比沟槽结构(由 Puurunen 及其同事开发,由芬兰 VTT 技术研究中心提供)进行比较,沟槽呈水平方向。图 4 展示了这种 PillarHall™ 结构。在以下动画中,蓝线绘制了气相反应物密度(从 0 到 1)。表面覆盖率θ 最终决定了沉积膜的厚度,在沟槽表面上以红色轮廓表示。
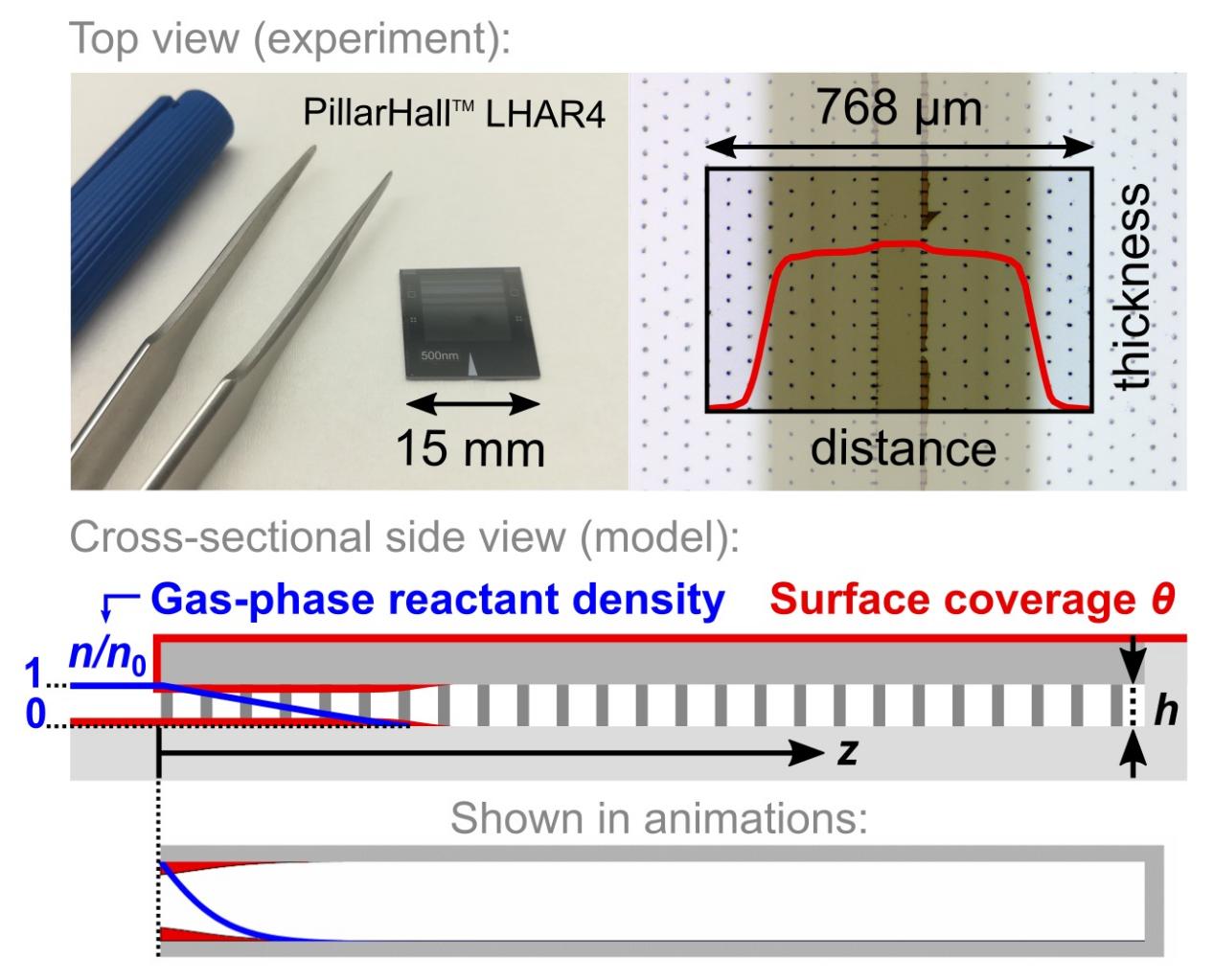
图 4:在实验中使用的由 VTT 提供的 PillarHall ™水平沟槽结构图片(顶部),其中硅膜被移除,沉积的薄膜可见。结构的示意横截面(中间)显示了气相反应物密度(蓝线)和表面覆盖率(红色轮廓)。
第一个动画,其中 S0AR2=0.01,对应于反应限制生长。为了完整地表示生长过程,此动画分为“短时间尺度”部分和“长时间尺度”部分。在现实生活中,这些阶段分别大约需要微秒和秒,具体取决于实验条件。在短时间尺度部分,我们可以看到蓝线移动到沟槽中,直到它在各处具有相同的值。这对应于气相反应物分子扩散到沟槽中,直到它们均匀分布。在长时间尺度部分,我们可以看到这导致表面覆盖率均匀增加,如红色轮廓所示。
.gif)
动画 1:模拟反应限制生长,其中 S0AR2 =0.01。在本博客文章的所有动画中,红色轮廓代表表面覆盖率,蓝线代表沟槽内的气相反应物密度。此外,底部还包含一条小时间线,以指示动画的进展。
由于反应限制生长过程中生长速率均匀,高 AR 结构中达到薄膜饱和所需的反应物剂量与平面基底相同。相应地,饱和剂量与成正比 1/S0A0,其中 A0 是每个吸附位点的平均有效面积。在图 1 和 3 中,该面积A0对应于一个正方形的面积,代表一个吸附位点。
下一个动画对应于扩散限制生长。在这里,S0AR2=1000 反应物分子在扩散到沟槽深处之前就已经吸附了。因此,薄膜在入口附近达到饱和,而沟槽内部深处的表面仍然是“空的”。随后,在入口附近的饱和区域中,反应物分子不再通过吸附而损失,因此可以扩散到仍有空吸附位点的“吸附前沿”。因此,薄膜生长越来越深入沟槽。
(3).gif)
动画 2:模拟扩散限制生长 S0AR2=1000。
请注意,沉积膜的穿透深度不是由反应物分子扩散的时间决定的,而是由供应到沟槽中的反应物分子的数量决定的。这是因为吸附位点必须“填满”才能达到此深度,如图 3(右)所示,为此也需要一定数量的反应物分子。因此,穿透深度与反应物剂量成比例,即反应物压力乘以剂量时间。这不是线性关系,因为并非每个在沟槽内随机扩散的分子都会到达吸附位点:它也可以移出沟槽。由于这种随机游走扩散,沉积膜的穿透深度与 PD50% ∝ h(√A0Dose)成比例,其中PD50%是所谓的半厚度穿透深度。请注意,当 A0 较大时,表面上需要填充的吸附位点较少,沉积膜的穿透深度也更深。
扩散限制生长期间沉积薄膜穿透深度的表达式也可用于预测饱和剂量Dosesat,因为当穿透深度PD50%与沟槽的总长度L相同时,大约达到饱和状态。因此,h√(A0Dosesat) ∝ L,利用纵横比 AR=L/h,可以得出Dosesat∝(1/A0)AR2。请注意,这里的饱和剂量不受反应物反应性的影响,而仅受纵横比和吸附位点数量的影响。这解释了 Gordon 模型在假设粘附概率为 1 的情况下成功预测扩散限制生长的饱和剂量的原因。
虽然初始粘附概率的值不会影响扩散限制生长过程中的穿透深度,但它会影响覆盖轮廓的形状,下面给出的动画说明了这一点。其中表面覆盖率作为缩放距离Z/L进入沟槽的函数绘制。如果气相反应物分子非常“粘”,它们最有可能直接吸附在吸附前沿,在那里它们首先遇到空吸附位点。相反,如果值 S0 较低,反应物分子在吸附之前可以更频繁地四处散射,从而使吸附前沿更加分散。请注意,这种前沿的“锐度”与反应物剂量保持不变,并且在第一次近似中仅由 S0决定。因此,可以使用该关系通过实验确定与穿透深度的半周期相对应的值,如 Arts, K 的论文“从它们对薄膜保形性的影响中提取 Al2O3 原子层沉积过程中 H2O 和 Al(CH3)3 的粘附概率”中所述。
(4).gif)
动画 3:在扩散限制生长过程中,对于不同的初始粘附概率值,表面覆盖率与进入沟槽的距离的关系。
03.等离子体 ALD:复合限制生长
对于等离子 ALD,保形性问题变得更加困难。如“模拟 ALD 保形性”部分所述,扩散到沟槽中的等离子自由基也可能通过复合而损失,如表面复合概率所示r,而不仅仅是通过吸附。复合损失的存在通常会导致复合限制生长,其中反应物(此处为等离子自由基)进入高 AR 结构的渗透深度受到复合的限制。
为了确定薄膜生长是否是复合限制的,可以使用 rAR2的值。类似于前面部分讨论的参数S0AR2,rAR2的值代表扩散时间和复合时间之间的比率。当 rAR2 ≥1 时,等离子体自由基在它们能够扩散到沟槽末端之前就复合了,使得薄膜生长受到复合限制。当 rAR2 ≤ 1时,等离子体自由基可以到达沟槽的末端,并根据 S0AR2 的值提供反应限制或扩散限制生长。请注意,在这种情况下,沉积薄膜的穿透深度可能受到前体半周期的限制,而不是等离子体半周期。
在以下动画中,我们可以看 rAR2 的值如何影响薄膜生长。这里,S0AR2 保持在 1000 恒定,rAR2 从100变化到1000和10000,使得在所有三种情况下薄膜生长都受到复合限制。最引人注目的是,可以看到等离子体自由基的穿透深度,因此沉积薄膜的穿透深度对于较低的复合概率值更高。对于 rAR2 = 100,薄膜生长最终达到沟槽的大约一半,而对于 rAR2 = 10000,只有结构的前 5%被涂层包覆。作为一个经验法则,当 rAR2 ≈ 1 时,仍然可以相对容易地涂层高 AR 结构。或者换句话说,可以在等离子体 ALD 过程中轻易达到的纵横比可以通过 AReasy ≈ 1/√r估计。在我们的工作中,我们确定 𝑟 ≈ 6 × 10-5用于等离子体 ALD 的 SiO2 和 TiO2,因此使用扩展的等离子体步骤实现了高达 AR ≈ 900 的薄膜生长。这表明等离子体 ALD 也可以产生非常共形的薄膜。
(1).gif)
动画 4:不同值和固定值的复合限制生长模拟 S0AR2
让我们更仔细地看看复合限制生长期间的总体生长行为。再次,上面显示的动画被分成两部分。在“短时间尺度”部分,自由基扩散进入沟槽,并通过吸附反应和复合反应同时丢失到侧壁。在“长时间尺度”部分,我们可以观察到复合损失如何影响薄膜生长。首先,在沟槽入口附近的区域达到了表面覆盖率的饱和。由于在该饱和区域不再发生吸附损失,自由基可以更深入地进入沟槽。尽管如此,复合损失继续进行,也在饱和表面上,因此最终限制了自由基可以扩散的深度。在这一点上,形成了进入沟槽的自由基通量和通过表面复合持续丢失自由基之间的平衡。这种平衡导致自由基密度的稳态指数衰减,如蓝线所示。
请注意,当S0AR2 ≤ rAR2 时,复合损失立即占主导地位,所以也在沟槽开始处表面覆盖率达到饱和之前。尽管如此,迟早也会得到同样的自由基密度指数衰减,当 S0AR2 > rAR2时,正如下面所示的动画所示。因此,S0AR2 的值影响覆盖率轮廓的形状,但在复合限制生长期间对沉积薄膜的穿透深度影响相对有限。
(1).gif)
动画 5:模拟固定值 rAR2 和非常不同的值的复合限制生长 S0AR2
自由基密度的指数衰减有几个实际后果。正如已经提到的,它限制了可以相对容易涂层的纵横比(AReasy≈ 1/√r)。也可以达到更高的纵横比,但需要成指数级的时间来实现高AR结构内部更深的薄膜饱和。因此,达到整个结构饱和所需的剂量时间随着纵横比的增加而指数增加。此外,沉积薄膜的穿透深度与自由基剂量对数增加。这种关系可以用来实验确定 的值,如我们的论文“等离子体辅助原子层沉积 SiO2、TiO2、Al2O3 和 HfO2 期间薄膜共形性和提取的 O 原子复合概率”中解释的。
总结
我们希望这篇博文有助于解释和理解(等离子) ALD 过程中保形薄膜的生长,同时,也向大家分享以下几条经验:
1粘附概率和表面复合概率是决定(等离子)ALD 过程中薄膜保形性的重要参数。
2与吸附相反,表面复合是持续存在的,因此往往成为等离子体 ALD 过程中活性物质的主要损失通道。
3对于表面复合概率较低的工艺,等离子 ALD 也可以提供出色的薄膜保形性。
参考文献
【1】K. Arts, W.M.M. Kessels and H.C.M Knoops. Basic insights into ALD conformality – A closer look at ALD and thin film conformality. 2020, 1. AtomicLimits.
【2】Arts, K.; Vandalon, V.; Puurunen, R. L.; Utriainen, M.; Gao, F.; Kessels, W. M. M. (Erwin); Knoops, H. C. M. Sticking Probabilities of H2O and Al(CH3)3 during Atomic Layer Deposition of Al2O3 Extracted from Their Impact on Film Conformality. J. Vac. Sci. Technol. A 2019, 37 (3), 030908.
【3】Arts, K.; Utriainen, M.; Puurunen, R. L.; Kessels, W. M. M.; Knoops, H. C. M. Film Conformality and Extracted Recombination Probabilities of O Atoms during Plasma-Assisted Atomic Layer Deposition of SiO2, TiO2, Al2O3, and HfO2. J. Phys. Chem. C 2019, 123 (44), 27030–27035.
【4】 Knoops, H. C. M.; Langereis, E.; van de Sanden, M. C. M.; Kessels, W. M. M. Conformality of Plasma-Assisted ALD: Physical Processes and Modeling. J. Electrochem. Soc. 2010, 157 (12), G241–G249.
【5】Cremers, V.; Puurunen, R. L.; Dendooven, J. Conformality in Atomic Layer Deposition: Current Status Overview of Analysis and Modelling. Appl. Phys. Rev. 2019, 6, 021302.
